2.9. Atmung und Beatmung#
2.9.1. Atemphysiologie#
Das normale Ventilations-Perfusions-Verhältnis ist 1:1, Kontaktzeit des Blutes in Ruhe 0,75 s, bei Lungenkranken mit verdickter Basalmembran ist dies vor allem bei Belastung zu kurz → Dyspnoe.
Sauerstoffbindungskurve ist sigmoidal (SO₂ oben und paO₂ rechts). P50 ist der Wert, bei dem Hb zu 50% gesättigt = normalerweise paO₂ von 27 mm Hg.
- Rechtsverschiebung (Bohr-Effekt)
bei Azidose, Fieber, Hyperkapnie mit leichterer O₂ Abgabe ans Gewebe.
- Hüfnersche Zahl
1 g Hb kann 1,39 ml O₂ binden.
- Hypoxämie
vermind. paO₂ (bei vermind. Hb falsch hohe Sättigungswerte). Zyanose = SaO₂ vermindert (zentrale Zyanose bei > 5 g% nicht oxygeniertem Hb).
- Respiratorischer Quotient RQ
CO₂-Produktion: Sauerstoffaufnahme = 0,8 normal
- Oxygenierungsindex (Horowitz-Index)
paO2/FiO₂ = normal > 450
Zellatmung in den Mitochondrien: ATP mit O₂ + Glucose erzeugt.
- Aerober STW
Funktionsstoffwechsel: Glucose – Pyruvat – CO₂ + H2O + 38 ATP
- Anaerober STW
Strukturstoffwechsel: Glucose – Pyruvat – Milchsäure + 2 ATP = keine Funktion mehr möglich, nur die Zelle hält sich für kurze Zeit am Leben = ZNS Eintrübung, Bradykardie,…
- Nicht respiratorische Funktion der Lunge
autokrin/endokrin = Hormonmodulation mit Bildung von Prostaglandin, Surfactant , Substanz P, Inaktivierung von A + NA, Sekretion von IgA, Regulierung des Säure/Basenhaushaltes, Phagozytose, Abbau über Cytochrom P450 in der Lunge. = Blutfilterung, Immunabwehr, Partikelfilterung und –abtransport.
- Schnellregulation der Atmung
Karotis-Sinus-Körperchen = periphere Chemorezeptoren melden O₂ und CO₂-Gehalt ans ZNS = Steigerung des AMV um 2-3l bei 1 mm Hg CO₂-Anstieg.
Langsame Regulation der Atmung über zentrale Chemorezeptoren in PONS, Medulla.
Prüfung:
Fluss/Volumen Kurve bei Spontanatmung aufzeichnen können!
Spirometrie: VT, IRV, ERV = Vitalkapazität
Körperplethysmographie (Heliumdilutionsmethode misst RV + FRC)
Totalkapazität = Vitalkapazität + RV
FRC = ERV + RV (lageabhängig, daher FRC auch lageabhängig!)
Verschlusskapazität/ closing capacity ist normalerweise < FRC = RV + Closing volume
Closing volume / Verschlussvolumen = Restvolumen in den Alveolen nach Expiration das die Alveolen offen hält
- Surfactant
reguliert Oberflächenspannung: in kleinen Alveolen niedrige OFSP damit sie leichter aufgehen + in großen Alveolen hohe Oberflächenspannung, damit sie nicht überdehnt werden.
Compliance, Resistance#
- Compliance
Dehnbarkeit (Volumen/Druck-Beziehung) von Lunge und Thorax, 1,5 ml / mbar / kg normal, ARDS ↓
- Resistance
Strömungswiderstand (Druck/Flow-Bez) erhöht durch Tubus, Sekret, …
Prüfung: Druck/Volumen-Kurve (Compliance) aufzeichnen können (sigmoidaler Verlauf):
- OIP
max. Alveolardehnbarkeit
- UIP
Alveolarverschlussdruck
Linearer Teil = Spontanatmung
Prüfung:
Lungenvolumina (IRV, VT, ERV, RV, VK, TK, FRC) kennen!
- Adaption bei Belastung
CO (SV x HF) steigt (und damit auch CI (ml / min / m²)); AMV (TV x AF) steigt ab > 30 vor allem Totraumventilation mit rascher Erschöpfung.
DO₂ steigt: DO₂ = HZV x Hb x SO₂ x 1,34 x 10 (normal 750 ml / min / m²)
Kritischer DO₂ ist 300, darunter anerober STW; VO₂ in Ruhe 3 ml / kg / min (bei Kindern und Kranken 5 x so hoch, 1°C Anstieg hebt VO₂ um 10%)
- West-Zonen
I apikal V>Q kein Fluss II intermitt. Fluss mit pulm. Art. Druck > Alveolardruck III kontinuierlicher Fluss basal da art. Und ven. Pulm. Druck > Alveolardruck V/Q = 0,8 (0 bei Shunt, ∞ bei Totraumventilation) = Perfusion ist größer als die Ventilation im Durchschnitt.
- Hagen-Poiseuille-Gesetz
Formel: Hagen-Poiseuille-Gleichung
\[ \dot{V} = \frac{\pi \cdot r^4 \cdot \Delta p}{8 \cdot \eta \cdot l} = \frac{\Delta p}{R} \]\(\dot{V}\): Volumenstromstärke
\(r\): Radius
\(\Delta p\): Druckunterschied
\(\eta\): Viskosität
\(l\): Länge
Strömungswiderstand ist proportional zur Länge und umgekehrt proportional zur 4 Potenz des Radius (Der Widerstand steigt mit der Länge und mit der vierten Potenz der Gefäßverengung).
Medizinische Bedeutung:
Vasokonstriktion, Stenosen → drastische Zunahme des Widerstands
Blutdruckregulation
Atemwegswiderstand bei Asthma oder COPD
Gefäßzugänge: Praktisch ist ein kurzer Venflon besser als ein Schenkel des ZVK mit gleichem Durchmesser.
Atemweg: Je größer der Tubus-Innendurchmesser, desto leichter das Weaning. Cave: Kindertubusdicke!
- Laplace-Gesetz
Beziehung zwischen Wandspannung, Dicke der Wand und den auf sie einwirkenden Druck.
In einem kugelförmigen Tropfen mit Radius \(r\) herrscht aufgrund der Oberflächenspannung \(\gamma\) an der Grenzfläche Flüssigkeit/Gas ein um \(\Delta p\) erhöhter Druck:
Formel: Laplace-Gesetz
\[ \Delta p = p_\text{innen} - p_\text{aussen} = \frac{2 \cdot \gamma}{r} \]\(r\): Radius
\(p_\text{innen}\), \(p_\text{aussen}\): Innen-/Außendruck
\(\gamma\): Oberflächenspannung
Anwendung:
Ohne Surfactant: bei Exspiration verlieren die Alveolen an Radius → Druckdifferenz an Alveolarwand in kleineren Alveolen nimmt stärker zu als in den größeren → die kleinen Alveolen entleeren sich in die größeren und kollabieren → Atelektase.
Surfactant setzt die Oberflächenspannung umso mehr herab, je weniger die Alveolen gedehnt sind → hält die Druckdifferenzen konstant
Recruitment-Manöver: kollabierte Alveolen habe einen kleinen Radius und brauchen viel Druck um sich wieder zu öffnen!
- Euler-Liljestrand-Mechanismus
bei herabgesetztem paO₂ in den Pulmonalgefäßen kommt es zur hypoxischen pulmonalen Vasokonstriktion = Ursache des Lungenödems in großer Höhe. Führt bei regionaler alveolärer Hypoventilation zu Vasokonstriktion mit therapieresistenter Oxygenierungsstörung. (ARDS)
2.9.2. Respiratorische Insuffizienz#
(paO₂ ↓) oder globale Insuff. (paO₂ ↓, paCO₂ ↑)
- Hypoxische respiratorische Insuffizienz
Oxygenierungsstörung bei Höhenaufenthalt oder luftgebundene Transporte (vermind. piO2/Hypoxie/HPV/Atelektasen), Hypoventilation bei Versagen der Atempumpe, Intrapulm. Re-Li-Shunt (HPV, Atelektasen), V/Q-Mismatch, pulmonale Hypertension, Diffusionsstörung (Ödem, Fibrose, massive HZV-Erhöhung mit Kontaktzeitverkürzung, red. pulm. Blutvolumen)
Therapie: FIO₂ und PEEP-Erhöhung + Ursache beheben
- Hyperkapnische respiratorische Insuffizienz
CO₂-Eliminationsproblem durch Störung des zentralen Atemantriebs (Med, Intoxikation, SHT, Meningitis), Störung der Nervenleitung (Querschnitt, Guillain-Barré, Phrenikusparese), Störung der neuromuskulären Weiterleitung (Myasthenia gravis, Muskeldystrophie, Relaxanzüberhang, Elektrolytstörung), Störung der Atemmechanik (Hämatothorax, Pneu, Erguss, Skoliose, Serienrippe), Obstruktive AW-Erkr. (Asthma, COPD, Tracheomalazie), Behinderung der Atemexkursion (Adipositas, erhöhter IAP)
Therapie: NIV/Beatmung, Ursache beheben, VT und AF erhöhen.
Hyperventilation ist ein wichtiger Kompensationsmechanismus um den alveolären paO₂ zu steigern und so durch den größeren Partialdruck die Oxygenierung zu verbessern und Hypoxämie zu verhindern.
- Parenchymversagen
ARDS, hypoxische respiratorische Insuffizienz.
- Pumpversagen
COPD, hyperkapnische respiratorische Insuffizienz.
2.9.3. Beatmungsformen#
Breath to breath support (jeder getriggerte Atemzug des Patienten wird vom Respirator durch positiven Druck unterstützt): PSV, ASB, PPS, NAVA z.B. bei COPD
Augmentierte Atemhilfen (intermittierende maschinelle Atemhübe zur Augmentation des AMV mit simultaner Spontanatmung, der spontane Atemhub erfährt keine Druckunterstützung): BIPAP, APRV, SIMV z.B. bei ARDS, intraoperativ bei Eingriffen ohne Relaxierung möglich (Voraussetzung: keine Lungenpathologie, kreislaufstabil, temperaturstabil)
Kontrollierte Beatmung: PCV, VCV, CMV, IPPV, CPPV
- Step by step approach
Atemtherapie (Triflow, physikalische Therapie)
CPAP-Maske
Intubation: BIPAP, ASB, PSV mit PEEP + ev. IRV
Lagerungstherapie, NO-Inhalation, ILA, ECMO
Spontanatmung = neg. Druckatmung; Beatmung = positive Druckatmung (dorsales ZWF starr)
- VCV
Freiheitsgrad = Spitzen (Tubuswiderstand)- und Plateaudruck (Alveolardruck), der Alveolardruck kann nur in den No-Flow-Phasen gemessen werden! Stenose (Tubusknick) erhöht Spitzendruck bei unverändertem Plateaudruck. Compliance-Verminderung (z.B. Kopftieflage) vermindert VT, sodass Spitzen und Plateaudruck erhöht werden müssen.
- PCV
Freiheitsgrad TV; konstanter endexpiratorischer Druck (Plateaudruck) ohne Spitzendruck, mit dezelerierendem Flow. Complianceverminderung: VT sinkt AMV sinkt CO₂ steigt Frischgasflow/min wird dem System zugeführt (nicht Beatmung). Z.B. Bei Flow 1 l und AMV 5 l werden 4 l wiederverwendet. Bei minimal Flow Anästhesie < 0,5 l muss FiO₂ erhöht werden! (mind. 75%).
- Toxische Sauerstoffwirkung bei > 0,4 FiO₂
Erhöht Sauerstoffradikale mit erhöhter Permeabilität/Ödem, Zerstört Surfactant, aktiviert Makrophagen und Granulozyten, Stört Zilienfunktion.
Resorbtionsatelektasen bei hohem paO₂ in der Alveole = viel O₂ geht ins Blut, der Partialdruck der in der Alveole verbleibt ist unter dem hydrostatischen Druck der Umgebung = Atelektase.
- PEEP
Physiologisch 5-10 mm Hg in der Trachea nach Expiration, durch Tubus verhindert. PEEP verschiebt VT nach oben (red. IRV) und hebt damit die FRC
AZV = Totraumventilation (va. Bei AF > 30 / min) und Frischluftventilation!!
Die Höhe des PEEPs richtet sich nach der Hämodynamik, KG, Lagerung des Patienten!
- Inspirationszeit
BIPAP = zeitgesteuerte Tinsp; ASB = flussgesteuerte Tinsp (Spitzenfluss sind 100% bei 25% Ende der Inspiration). Eine Verlängerung der Inspirationszeit verlängert Verbessert die Oxygenierung (IRV).
- AF
Ist abhängig vom absoluten KG (z.B. Mann mit 180 cm / 50 kg hat herabgesetzte AF), Temperatur, CO₂-Produktion (Sedierung reduziert CO₂-Produktion im Gehirn daher AF erniedrigt!)
- RAMPE
Normalerweise 0,2 s; Ziel ist eine vollständige Inspiration in der Inspirationszeit mit kurzer NOFlowphase vor Exspiration. Bei zu raschem Anstieg kann es zu reflektorischem Pressen mit hohem Spitzendrücken kommen.
- Flowtrigger
normalerweise 2 l / min = Wenn der Patient > 2l/min einatmet bekommt er eine Druckunterstützung. Entscheidend ist die Einatemgeschwindigkeit!!
2.9.4. Weaning#
= Übertragen der Atemarbeit vom Respirator auf den Patienten.
Prinzipiell 2 Möglichkeiten:
Kontinuierlich: augementierte Beatmungsformen mit stufenweiser Reduzierung
diskontinuierlich: T-Tube-Trials = steigende Dauer (Feuchte Nase mehrmals täglich, bei 2h, Extubation) = SBT Spontanes breathing Trial (Zeit von Anfangs 30 min an feuchter Nase steigern bis 120min)
Wann kann mit dem Weaning begonnen werden?
- Weaningkriterien
Hämodynamik stabil, keine oder nur niedrigdosierte Katecholamine
Kompensierter Infekt (kein Fieber)
Keine geplante OP mehr
Keinen ausgeprägten Meteorismus
Säure/Basen-Haushalt in Ordnung pH >7,3
Elektrolyte im Normbereich (Mg, Ca, K!)
Ausreichende Wachheit und neurologische Stabilität
Respiratorisch: suffizienter Atemapparat (z.B. bei instabilem Thorax,…), OI > 200, PEEP 5-10, VT ausreichend, BGA + SO₂ in Ordnung, RSBI<105 (f/VT), Atemwegsokklusionsdruck < 6
SaO₂ ≥ 90% bei FiO₂ ≤ 40% und PEEP ≤ 8 mbar
- Atemwegsokklusionsdruck P0,1
Maß für den zentralen Atemantrieb unter Spontanatmung. Die Maschine verschließt für 100ms das inspiratorische Ventil und bestimmt den Druck. Normal ist 14 mbar. Bei > 6mbar Gefahr des Weaning-Versagens.
- Absolute Kontraindikationen
Optimal/Minimal Handling
Cerebro-protektives Handling
Warum lässt sich der Patient nicht weanen?
- Mögliche Ursachen eines Weaning-Versagens
Psyche: Delir, Panik
Herz: KHK, Herzinsuffizienz mit Decompensation, Vitien (unter Spontanatmung steigt das preload und sinkt das afterload mit erhöhtem Sauerstoffbedarf des Herzens = kardialer Stress!)
Atmung: verminderte Compliance, erhöhte Resistance, erschöpfte Atemhilfsmuskulatur, paradoxe Atmung/instabiler Thorax, Rapid S.Breathing
Andere Ursachen: z. B. Sedierungproblematik (Tubustoleranz vs. Atemantrieb), Hypersekretion
Das Weaning muss abgebrochen werden, wen die AF > 35 / min mit SO2<90% bei unverändertem FIO₂ bleibt, HF > 140 / min oder < 50 / min, RRsyst. > 180 oder < 70 mm Hg, vegetative Symptomatik (schwitzen, Übelkeit,…), paradoxe Atmung, Atemnot! Ein erfolgreiches Weaning liegt vor, wenn der Patient 48 h Spontanatmung zeigt ohne respiratorische Erschöpfung.
- Ursache beheben
Weaning induzierte kardiale Dysfunktion: mit neu aufgetretenem Lungenödem, Ischämiezeichen im EKG, reduzierter EF.
Therapie mit Entwässerung, Nitroglycerin iv 40-600 µg / min.
Überlastete Atemmuskulatur mit Schaukelatmung: mit schwachem Hustenstoss, Sekretstau, und paCO₂-Anstieg.
Therapie: antiobstruktive Medikamente, Entwässerung, Pleurapunktion. Prävention: früher Spontanatemmodus, wenig Sedierung, frühe Rehabilitation.
Wann kann der Patient extubiert werden?
- Extubationskriterien
Screening der respiratorischen Funktion: OI > 200, PEEP 5-10 cm H₂O, wach, Schutzreflexe, keine relevanten vasoaktiven Medikamente mehr?
AF < 35 / min, VT ausreichend ? BGA, SO2
Eine zu frühe Extubation führt zur Reintubation, eine zu späte Extubation führt zur VAP oder Selbstextubtion.
- BIPAP
Sedierung stoppen, AF in 2er Schritten reduzieren, CO₂ Ansteigen lassen, PEEP erst unter 10 reduzieren, wenn FIO2< 0,4 ist! Zur Extubation muss der Patient wach sein, Schutzreflexe haben (husten, Aufforderung befolgen) und AF > 5 / min sein! Keine Reduktion der Druckunterstützung, da es nur zu vermehrter Totraumventilation kommt, wenn VT < 250 ml wird!
- ASB
Druckunterstützung in 2er Schritten reduzieren bis ca. 5; Extubation des wachen Patienten mit Schutzrefelxen ev. CPAP bei PEEP > 5
Weaning bei COPD: Extubation + Anschließend NIV! CPAP-ASB, PSV-ASB, PPS
ATC = automatische Tubuscompensation
RSBI (= rapid shallow breathing index): f/VT < 105 beim Weaning = hohe AF und niedriges VT mit acuter respiratorischer Azidose = Atemzüge/min durch das Titalvolumen in Litern = Ein Maß für das Verhältnis von Belastung und Kapazität der Atemmuskulatur.
Smart Care: Spontanatmung im ASB-Modus Unterstützungsdruck nach Frequenz, Tidalvolumen und etCO2
Smart Care vs. ASB im Weaning: smart care im postoperativem Einsatz gefahrlos anwendbar.
ASB: Weaningdauer ist Personalabhängig.
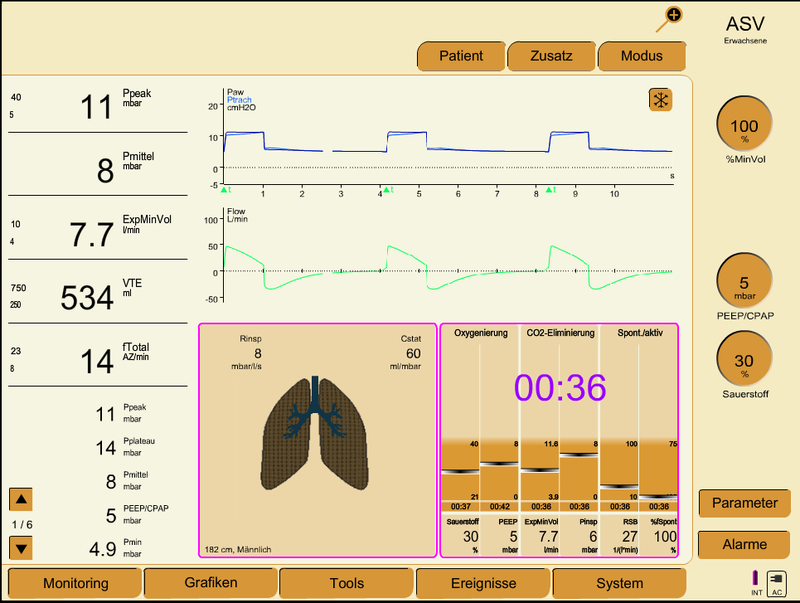
Fig. 7 Patient im ASV-Modus mit voller Spontanamtung. Eine Umstellung in den Spontanmodus bietet sich an.#
(Beatmungsgerät: Hamilton G5)
2.9.5. Nicht invasive Ventilation NIV#
Vorraussetzung: ausreichend wacher, kooperativer Patient mit Schluck-, Husten- und Würgereflex, da kein gesichterter Atemweg!
- Vorteil
keine Intubationskomplikationen, red. VAP, keine Sedierung nötig, verkürzter Intensivaufenthalt.
- Masken
Nase, Mund/Nase, Full-Face, Helm, Mundstücke
- Probleme
Leckage!!!, Personalintensiv, kein gesichterter Atemweg, SH-Schwellung
- Indikationen
COPD-Exazerbation
first level: kardiales Lungenödem
akute respiratorische Insuffizienz (bei immunsuprimierten Patienten)
Thoraxtrauma mit Serienrippe (Vorraussetzung Bülau bei Pneumoth.)
Postoperative Atelektasen (pulmonale Funktionseinschränkung va. Schmerzbedingt)
Weaning beim COPD-Patienten, Herzinsuffizienz, paCO₂ > 45 mm Hg vor der Extubation, Sekretproblemen bei vermindertem Hustenstoss, Nachwirkungen einer Anästhesie, erhöhtem Intraabdominellen Druck, nach Thorax und Oberbaucheingriffen.
Respirator muss Leckage-Kompensation und ausreichend Flow bieten.
- Kontraindikationen
Pat. ist nicht wach mit Schutzreflexen (Koma, Delir), Hämodynamische Instabilität/maligne Arrhythmien, Gesichtsschädelverletzungen/deformationen, NICHT drainierter Pneumothorax, massive Sekretproduktion;
Ausnahme: hyperkapnisches Lungenversagen mit CO₂-Narkose trotzdem NIV
- NW
Läsionen der Nase, Irritationen der Augen, Austrocknen der SH
- Erfolgskriterien
paCO₂ sinkt, paO₂ steigt, AF und HF sinken, Klinische Besserung (Angst, Dyspnoe, usw.), Besserung nach 20 min!!
- Abbruchkriterien
weitere Verschlechterung der respiratorischen Insuffizienz, zunehmende Eintrübung, Hämodynamische Instabilität, Arrhythmien, Maskenintoleranz, RSBI (f/VT)
2.9.6. Narkoserespiratoren#
- Atemkalk
Pillenkalk (NaOH, Ba(OH)₂ ), bindet CO₂, wärmt und befeuchtet Gas, Ablaufdatum wegen Austrockung beachten! (Problem bei Kindern zu wenig CO₂-Abgabe, damit zu wenig Befeuchtung und Erwärmung des Gas = bei langer OP externe Geräte empfohlen!)